Neurociencia
En búsqueda de un sitio de acción para el efecto central de los analgésicos no opioides
El aporte de nuestro laboratorio
Desde hace más de una década, nuestro grupo de investigación ha venido estudiando la manera como los analgésicos producen su efecto a nivel central. Una de las estructuras que ha sido blanco de nuestro interés es precisamente la SGPA y, en especial, la forma en la que su manipulación permite la activación del sistema endógeno para el control nociceptivo, promoviendo así el cierre de la llamada "compuerta del dolor" que opera a nivel espinal.
Existen evidencias de que los efectos analgésicos de la SGPA son canalizados a través de un relevo en la formación reticular bulbar. Allí se encuentras las llamadas células on y off de la región rostroventromedial (RVM) del bulbo raquídeo (Fields y col., 1983), que reciben conexiones desde la SGPA (Vanegas y col., 1984a) y envían sus axones al asta dorsal de la médula espinal (Vanegas y col., 1984b). La evidencia hasta ahora colectada indica que las células on facilitan y las células off inhiben, la transmisión nociceptiva a nivel espinal en ratas. Esto se pone en evidencia, por ejemplo, al administrar un opioide como la morfina, tanto por vía sistémica como mediante su microinyección en la SGPA. Estos tratamientos provocan una disminución del nivel de actividad de las células on, el incremento de la actividad de las células off y simultáneamente logran inhibir el RSC, lo cual se puede interpretar como una interferencia en la transmisión nociceptiva a nivel de la médula espinal, capaz de provocar antinocicepción (Fields y col., 1983).
 |
|
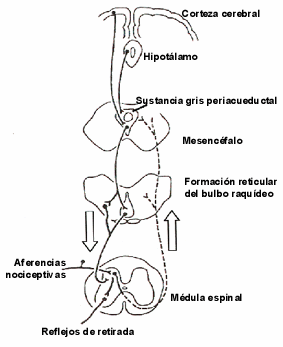
Figura 2. Diagrama esquemático del circuito de modulación descendente del dolor (flecha hacia abajo), el cual involucra como estructuras claves a la sustancia gris periacueductal del mesencéfalo y a la región rostroventromedial de la formación reticular bulbar. La activación de las neuronas de estos dos sitios es capaz de producir la inhibición conductual de las respuestas ante estímulos nocivos. En nuestro laboratorio hemos demostrado que los analgésicos no opioides son capaces de promover éste efecto como parte de su mecanismo de acción central. La flecha ascendente indica el sentido normal de conducción que sigue la información nociceptiva cuando un estímulo nocivo es aplicado en una región del cuerpo. |
Las células on y off de la RVM también están involucradas en el efecto central de los analgésicos no opioides. La administración de DIP o de lisina-acetilsalicilato en ratas (Tortorici y Vanegas, 1994; 1995), ya sea i.v. o por una microinyección en la SGPA, produce, al igual que la morfina pero en menor grado, una disminución en la actividad de las células on y una excitación de las células off, lo cual de nuevo es acompañado de una inhibición del RSC. Estos hallazgos sugieren que los analgésicos no opioides también son capaces de actuar sobre la SGPA, y que ésta, mediante su brazo eferente constituído por las células on y off de la RVM, es capaz de producir la inhibición temporal de la transmisión nociceptiva a nivel de la médula espinal. En un estudio ulterior, se logró demostrar que la microinyección de DIP en la SGPA produce una inhibición selectiva de las respuestas de las neuronas sensitivas espinales ante la aplicación de estímulos nocivos (Vanegas y col., 1977).
Pese a todos estos resultados, aún no está claro cuál es el mecanismo de acción de los analgésicos no opioides en la SGPA. Nuestro grupo maneja la hipótesis de que la acción de estos fármacos involucra la participación de los opioides endógenos. La primera evidencia en relación a esto surge del hallazgo de que la naloxona, un antagonista de opioides, al ser administrada por vía sistémica, o por microinyección en el mismo sitio de la SGPA donde previamente se inyectó DIP, produce una reversión parcial del efecto antinociceptivo de esta última, lo cual pone en evidencia la participación de los opioides endógenos presentes en la SGPA (Tortorici y col., 1996).
Más recientemente, y empleando para ello ratas despiertas a las cuales se les habían implantado cánulas permanentes mediante cirugía estereotáxica, se logró demostrar que la microinyección repetida de DIP en la SGPA genera tolerancia a su efecto analgésico, y más importante aún, tolerancia cruzada a una microinyección de morfina en el mismo sitio de la SGPA. En estos animales ahora tolerantes a la DIP, la administración de naloxona provocó la aparición de síntomas de abstinencia (Tortorici y col., 1999b). Esta disminución progresiva de la eficacia analgésica de la DIP es similar al estado de tolerancia que se produce al microinyectar morfina en forma repetida en la SGPA de ratas (Tortorici y col., 1999a).
Estas evidencias revelan similitudes en los mecanismos de acción de los analgésicos opioides y los no opioides. Además de su tradicional acción periférica, los analgésicos no opioides también actúan a nivel central. Es decir, junto a la clásica inhibición de la síntesis de PGs, también tiene lugar la puesta en marcha de un mecanismo descendente de inhibición nociceptiva, que involucra al eje SGPA-RVM-médula espinal, al parecer activado a través de la participación de los opioides endógenos y que promueve la inhibición de la transmisión nociceptiva, cerrando la "compuerta espinal". En este posible mecanismo, el blanco de la acción de los opioides (endógenos o exógenos) sería la inhibición local de interneuronas inhibitorias, que contienen ácido g-amino-butírico (GABA) y que estarían normalmente ejerciendo una restricción tónica del sistema endógeno para el control del dolor (Moreau y Fields, 1986; Vaughan, 1997).
Estos experimentos señalan la posibilidad de que en la práctica médica, la administración repetida de un analgésico no opioide pudiera inducir un estado de tolerancia cruzada con opioides, tanto endógenos como exógenos, y el riesgo de aparición del síndrome de abstinencia, lo cual tendría serias consecuencias tanto clínicas como sociales. |