La hepcidina (Hpc) es un péptido que fue
aislado de orina humana por Park y colaboradores en el 2001(1) y
que recibió su nombre con base a su lugar de síntesis (hepatocitos) y a su
comprobada propiedad antibacterial in vitro (-cidina). En el curso de estos estudios, uno de los donantes de
sangre desarrolló una infección sistémica y la concentración de hepcidina se
incremento 100 veces durante el proceso agudo. Esto, indicó que la hepcidina se
comportaba también como un reactante positivo de fase aguda (1).
Gracias a la
Espectrometría de Masa, este péptido pudo ser
caracterizado como un polipéptido de 25 aminoácidos (Hpc-25) cuya estructura
espacial, lo define como una lámina plegada ß, con 8 residuos de cisteína cuyos
brazos están unidos por 4 puentes disulfuro(2). La Figura 1 muestra
una representación de la molécula de hepcidina activa.
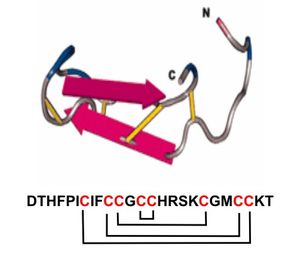
Figura 1. Secuencia
aminoacídica y modelo tridimensional de la hepcidina humana. Notas:
Los terminales carboxilo y amino están indicados por C y N, respectivamente.
Los puentes de disulfuro se muestran en amarillo. En la secuencia primaria
mostrada debajo de la figura, se señalan estos puentes, que unen sus 8 residuos
de cisteína (3).
La Hepcidina es una hormona peptídica
producida principalmente en el hepatocito y que al igual que otras hormonas
peptídicas, es sintetizada inicialmente como un péptido de mayor peso molecular,
la pre-prohepcidina de 84 aminoácidos que luego es transformada en prohepcidina
de 60 aminoácidos y finalmente en su forma activa hormonal de 25 aminoácidos.
La región N-terminal de la prohormona es la que está involucrada en su función
reguladora, por lo que la pérdida de aminoácidos asociada con su transformación
de pre-prohepcidina a prohepcidina y finalmente a hepcidina, proviene del
extremo carboxilo terminal. Estas transformaciones se producen en los organelos
de los hepatocitos (retículo endoplasmático y trans-golgi) durante la síntesis
y distribución de la hepcidina. La enzima que se encarga de estas
transformaciones es una pre-proteína convertasa especial conocida como furina y
que se sintetiza al mismo tiempo que se sintetiza la hepcidina. Inhibidores de
esta enzima como la α-1 antitripsina afectan la conversión intracelular de pre-prohepcidina
a prohepcidina, así como la transformación de la prohepcidina a su forma activa
en el plasma. La eliminación de los 5 últimos aminoácidos de la región N terminal
resulta en la pérdida de su función (4,5,6).
Inicialmente se pensaba que la hepcidina
era sintetizada exclusivamente en el hígado, sin embargo investigaciones
posteriores han demostrado que el gen de la Hpc (HAMP) también se expresa en tejidos extrahepáticos. Kulaksiz
y colaboradores (2005) (7) demostraron que la Hpc también está
presente en las células apicales de los túbulos del riñón de humanos, ratas y
ratones, y postularon que esta hormona puede tener una función a nivel del
riñón y del tracto urinario. Luego, Schwarz y
colaboradores (2012) (8) evaluaron la expresión y localización de la
hepcidina gástrica en ratones y reportaron que la hepcidina se encuentra de
manera abundante en el fondo y en el cuerpo del estómago y que tanto la
Interleukina 6 como la infección por H.
pylori sobreestimulan su expresión. Estos mismos autores observaron que en humanos
la expresión de la hepcidina gástrica aumentó durante la infección por H. pylori y se normalizó después de una
exitosa erradicación y concluyeron que la hepcidina es un producto de las
células parietales, que son las mismas que regulan la acidez gástrica y que se
han asociado con el desarrollo de la úlcera gástrica bajo condiciones de estrés.
Más recientemente, se ha reportado que la hepcidina se produce en astrocitos y
microglías en el cerebro (9), posiblemente en la glándula mamaria (10),
así como en macrófagos y adipocitos (11). Sin embargo, la producción
hepática es la más importante y sirve
para satisfacer las necesidades de esta hormona tanto en el hígado como para
enviarla a otras células blanco (12), como son los enterocitos
duodenales, el propio hígado y los macrófagos del tejido retículo endotelial,
encargados de la eritrofagocitosis y reutilización del hierro de los
eritrocitos senescentes (11).
A continuación se discuten los aspectos más
importantes de la síntesis de la hepcidina, su efecto sobre su receptor
natural, la ferroportina y la función de la hepcidina-ferroportina sobre el
metabolismo y homeostasis del hierro.Hepcidina y su papel
regulador en el metabolismo del hierro
Los primeros indicios sobre el papel
regulador de la hepcidina en el metabolismo del hierro aparecieron en los
estudios de Pigeon y colaboradores (2001)(13), quienes señalaron, que en ratones, la síntesis de la
hepcidina era inducida por el consumo de hierro y que este péptido se sobreexpresaba
ante una sobrecarga de hierro(13). Sin embargo, fueron los trabajos
de Nicolas y colaboradores (2001, 2002) con ratones transgénicos los que
mostraron el papel específico de la hepcidina sobre el metabolismo del hierro(14,15).
Estos investigadores observaron que en aquellos ratones donde se bloqueaba el
gen de la hepcidina, se desarrollaba una hemocromatosis con deposición de hierro
en hígado, páncreas y bazo (14), en contraste, en los ratones donde
se inducía una sobreexpresión del gen de la hepcidina, se desarrollaba una
anemia severa y la mayoría de las crías morían pocas horas después de nacer,
sugiriendo que la hepcidina inhibía la transferencia placentaria de hierro(15).
Estos estudios mostraron que la hepcidina es un péptido responsable de regular
tanto la captación de hierro a través del intestino como la liberación del
mismo por los macrófagos y los hepatocitos, el exceso de este péptido impide el
transporte de hierro a través del intestino y de la placenta y ocasiona una
carencia de hierro. En contraste, su deficiencia produce un aumento en la
absorción del hierro dietario, así como una sobrecarga del mismo en los
tejidos. Estos resultados llevaron a definir a la hepcidina como una hormona
que participa en la regulación del metabolismo del hierro. Esto se comprobó en
pacientes con hemocromatosis hereditaria (16).