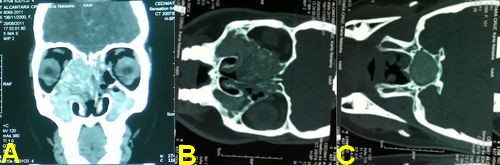
 Figura 1. TAC: Corte coronal de tomografía
axial computarizada que muestra ocupación de todos los senos paranasales. (B). TAC: Se observa desplazamiento de la lámina papirácea hacia la cavidad orbitaria derecha
desplazando el globo ocular. (C). TAC: Ocupación seno esfenoidal con afectación
de la lamina inter-seno
Figura 1. TAC: Corte coronal de tomografía
axial computarizada que muestra ocupación de todos los senos paranasales. (B). TAC: Se observa desplazamiento de la lámina papirácea hacia la cavidad orbitaria derecha
desplazando el globo ocular. (C). TAC: Ocupación seno esfenoidal con afectación
de la lamina inter-seno
La
paciente no presenta antecedentes familiares de co-morbilidad, no cirugías
previas, no traumas ni transfusiones. Dentro de las analíticas de laboratorio
cuentan un Hemograma, Plaquetas, Glicemia,
Creatinina TGO y TGP, examen de orina, coprológico, Tiempo de Protrombina, TPT,
dentro de los limites de referencias normales. Serología: VDRL, HIV, HBS-AG y HVC,
todos no reactivos, además una radiografía de tórax sin hallazgos patológicos,
con evaluación cardiovascular dentro de los parámetros normales. Previa
evaluación se decide su ingreso con fines de ser
llevada a cirugía. En Fecha 12/9/11, es llevada a quirófano con
Diagnostico pre quirúrgico de: tumor nasal vs. sinusitis micótica. Previas
medidas generales de asepsia y antisepsia, bajo anestesia general inhalatoria,
se introduce endoscopio de 30 grados en fosas nasales, se infiltra con
lidocaína + epinefrina, realizándose los siguientes procedimientos: antrostomía
maxilar amplia bilateral + etmoidectomía anterior y posterior bilateral + esfenoidotomía
bilateral con los siguientes hallazgos: Tejido marrón y verde de consistencia gomoso,
llenando antro maxilar etmoides y seno esfenoidal, degeneración polipoide de
cornete medio, engrosamiento de mucosa de senos paranasales y
lámina papirácea derecha segmentada y desplazada.
Se instaura
tratamiento con amoxicilina + acido clavulánico por 10 días La paciente es seguida con
chequeos a los 7, 21 y 60 días. Luego de
obtener el reporte de patología y cultivos micológicos se instaura tratamientos
antifúngicos con Voriconazol 200 mg por 3
meses.
El
tejido nasal extraído, fue dividido en dos
porciones: una para el estudio histopatológico y el otro para exámenes
microbiológicos y micológicos, obteniéndose los siguientes resultados:
a)
Examen directo: A los
exámenes en fresco del tejido se presentaron hifas tabicadas de color marrón claro a oscuro, las cuales fueron visualizadas al microscopio en
preparación con solución de Hidróxido de potasio (KOH) al 20%, con la coloración
de Gram y en forma tortuosas o de zig-zag con la coloración de
Grocott modificada, esta última es utilizada en nuestro laboratorio de Micología,
para todos las muestras clínicas sospechosas de hongos, ver figuras 2 y 3.
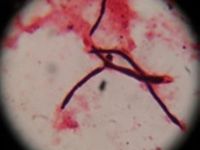 Figura 2 Se observan hifas dentro del tejido teñidas con coloración
de Gram.(100X)
Figura 2 Se observan hifas dentro del tejido teñidas con coloración
de Gram.(100X)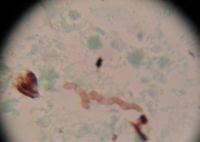
Figura 3 Preparación del tejido teñida
con coloración de Grocott, observándose la formación tortuosa o de zigzag.(100
X)
b)
Examen bacteriológico: En el examen bacteriológico
se reportó no crecimiento de
bacterias patógenas a las 48 horas de incubación.
Procedimiento para
cultivos: Los tejidos fueron troceadas con escalpelo
estéril en cabina de bioseguridad clase II y sembradas directamente en platos de Petri
conteniendo medios de Sabouraud cloranfenicol, Micobiotic Agar ambos incubados a 25˚C, y en
medio de Agar cerebro corazón el
cuál se incubó
a 37 ˚C. Los cultivos fueron chequeados
diariamente hasta el crecimiento de un hongo de micelio algodonoso al
principio blanquecino-marrón, de crecimiento rápido, que al cuarto día fue observado sobre los
fragmentos de tejidos y en todos los
medios, ver figura 4.
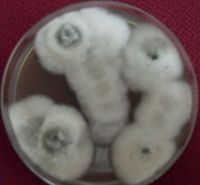
Figura 4 Crecimiento del hongo color Gris-marrón al 4to día en medio de
Sabouraud Cloranfenicol a 25 ˚C
c)
Macroscópicamente:
las colonias alcanzaron un diámetro de 4-8 cms. despues de ser incubadas a 25
˚C por una semana en Papa Dextrosa Agar, mostrando su madurez en 5 días. La superficie de las
colonias eran inicialmente blanca a gris marrón y luego olivo a negro cuando
envejecieron, el reverso eran también oscuras desde olivo a negro y de textura
aterciopelada ver figuras 5 y 6.
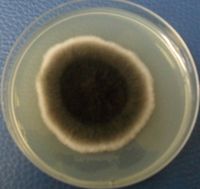
Figura 5. Colonias en Agar Papa con 5 días
de crecimiento. Se observan colonias de aterciopeladas con micelio de color
negro.
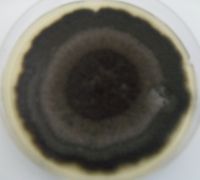
Figura 6. Colonia adulta con 7 días de crecimiento en Agar Papa a 25 ˚C
d) Micromorfología: en
una preparación del cultivo teñida con azul de lactofenol, se observó al
microscopio la presencia de hifas de
color marrón claro a oscuro, tabicadas y macroconidias oscuras ,septadas y
conidióforos geniculados . Para estimular la esporulación del hongo, se
procedió a preparar un microcultivo a
partir del aislamiento, en el medio
sólido Papa Dextrosa Agar (PDA), el cual
al cabo de 5 días de incubación se
observo al microscopio en preparación teñida con azul de lactofenol, hifas septadas
oscuras y conidias multiseptadas,
llamadas también poroconidias, con pequeño hilio, en forma de huso y de paredes gruesas, las cuáles
nacen desde los conidióforos geniculados,
como vemos en la figura 7.

Figura 7.
Microcultivo en Agar papa mostrando conidióforos
marrón claro, septados, geniculados y macroconidias septadas oscuras.(40X)
Las
conidias con septos de 3-5 se observaron en mayor cantidad y las que
tenían de 2 y 6 eran escasas. El
aislamiento fue identificado con todas las características de Bipolaris hawaiiensis, de acuerdo a la
descripción reportada por otros investigadores(7,8,12-14). Para establecer la diferenciación entre los géneros Bipolaris,
Exserohilium y Drechslera en el presente reporte se realizó un examen de
tubos germinales colocando un pequeño inóculo de la colonia del hongo aislado del
material clínico, en una lámina porta objeto con agua destilada y cubierto con
un cubre-objeto (todos en condiciones estériles), en donde a las 24 horas mostró
al microscopio, conidios de germinación bipolar e hilio recto a lo largo del
axis del conidióforo como se observa en la figura 8, verificándose como del
genero Bipolaris según describe Larone(8).
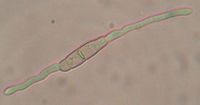
Figura
8. Obsérvese la germinación bipolar recta, con el test de tubos germinales a
las 24 horas.(40X)
Un subcultivo del hongo aislado, fue enviado a la Facultad de
Medicina de la Universidad de Rovira I Virgili,
departamento de Microbiología, donde se
confirmó su identificación como Bipolaris
hawaiiensis y fue incluida en la base de datos del cepario de la Facultad
de Medicina Reus colection (FMR), con el
# 12434, el 26-10-2012.
e) El estudio
histopatológico: De los cuatro
fragmentos de tejido de fosa nasal y
seno maxilar contenidos en frascos estériles con adición de formol, enviados al
laboratorio de histopatología, el mayor media 1.5 x 1.3 x 0.7 cms. Se reportó
inflamación crónica activa intensa con
predominio de eosinófilos, proliferación vascular, material amorfo con foco de calcificación,
fragmentos polipoides de mucosa respiratoria con edema e hifas cortas septadas.
Cuatro meses después
de la intervención quirúrgica se realiza tomografía control, (Figura 9), la
cual reveló cambios postquirúrgico en ambas fosas nasales y ligero
engrosamiento de la mucosa de seno
maxilar derecho.
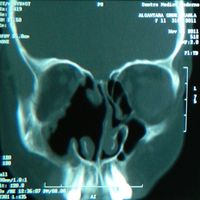
Figura 9:
TAC de nariz y senos
paranasales 2 meses luego del
procedimiento, mostrando cambios postquirúrgicos con ausencia de enfermedad de los senos paranasales.
Es llevada a
quirófano en fecha 6/2/12, para realizar revisión endoscópica y septoplastía +
Adenoidectomia, encontrándose los siguientes hallazgos: desviación septal ósea
y cartilaginosa hacia la izquierda, sinequia de cornete medio e inferior
izquierdo a septum, hipertrofia de adenoides, no se visualiza lesión micótica, sin embargo se toman varias muestras
de tejido para control, las cuales resultaron negativas a los cultivos para bacterias y
hongos. TAC de Seguimiento después de 23 meses postquirúrgico, (Figura 10).
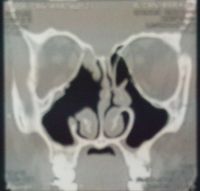
Figura 10. TAC de nariz y senos paranasales luego de 23 meses
post cirugía, mostrando cambios postquirúrgicos donde se observa el seno
maxilar libre de enfermedad sinusal