La B.
megalandra utilizada en
estos experimentos fue identificada por El Dr. Stefen Tillett del Herbario Ovalles
de la Facultad
de Farmacia de la Universidad Central
de Venezuela. Inicialmente medimos los efectos del extracto
acuoso de las hojas de B. megalandra (9)
sobre la neoglucogénesis de rebanadas de hígado de rata, incubadas en Krebs
Ringer bicarbonato suplementado con albúmina bovina saturada con oleato y
utilizando lactato o fructosa como substrato neoglucogénico. Como se puede
observar en la Tabla
1, la actividad neoglucogénica de las rebanadas controles es lineal hasta los
90 min. e igual con los dos substratos.

Tabla 1 Rebanadas de hígado de ratas ayunadas por 48 horas fueron
incubadas en 4ml de amortiguador Krebs-Ringer bicarbonato, suplementado con
albúmina de suero bovino saturada con oleato y usando lactato o fructosa como
substrato neoglucogénico, en la ausencia(control) o presencia de 9 UA264rm
del extracto de las hojas de B.
megalandra. En los tiempos indicados, en muestras del medio de incubación
se determinó la glucosa por el método de glucosa oxidasa-peroxidasa(29).
Los resultados se expresan en nmol de glucosa producidos/ mg de peso seco de
hígado y corresponden al promedio de 8-13 experimentos ± la desviación estándar.
Las diferencias observadas entre controles y tratadas con el extracto de la
planta fueron estadísticamente significativas a p<0.05 para fructosa y
p<0,005 para lactato.
En la presencia del extracto de la
planta ocurre una drástica disminución de la neoglucogénesis, siendo más
marcada a partir de lactato que de fructosa; estos resultados sugieren que en
el extracto de B. megalandra están
presente compuestos que bloquean dicho proceso en un punto más allá de la
entrada de ambos substratos. Como se muestra en la Tabla 2, cuando se usó G-6-P
como substrato de la G-6-Pasa
de microsomas intactos, el extracto foliar disminuyó de manera estadísticamente
significativa la VMAX
con una moderada elevación del KM sin afectar la actividad de la
enzima de microsomas rotos (9).
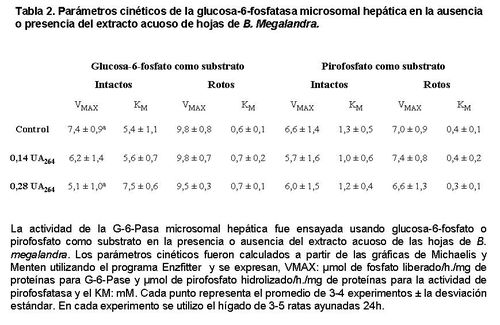
El extracto de la planta, no tuvo
efecto alguno cuando el substrato de la enzima fue PPi, tanto en microsomas
intactos como rotos; lo cual sugiere que el efecto del extracto de B. megalandra se ejerce sobre uno de los
transportadores del sistema de la
G-6-Pasa probablemente sobre T1 (9). Posiblemente
la inhibición de la neoglucogénesis hepática sea el resultado de la inhibición
de la G-6-Pasa
por los compuestos presentes en el extracto de la planta. Al medir el efecto
que durante el tiempo, ejerce el extracto de la planta sobre la actividad de la
enzima en microsomas no tratados (Figura 4) se observó que: en los controles la
actividad de la G-6-Pasa
fue lineal durante 30 min., en la presencia del extracto de B. megalandra la actividad de la enzima
también fue lineal hasta los 20 min. pero por debajo del control, después de
este punto ocurre una inflexión con una línea entre 20 y 30 min. con una
pendiente menor, sugiriendo que por efectos de la presencia del extracto foliar
probablemente se inhibe otro de los transportadores del sistema de la G-6-Pasa acumulándose los
productos de la reacción enzimática los cuales inhibirían la subunidad
catalítica (9). En vista de que los parámetros cinéticos de la G-6-Pasa usando PPi como substrato no fueron afectados por el
extracto de la planta, posiblemente el transportador inhibido sea T3.
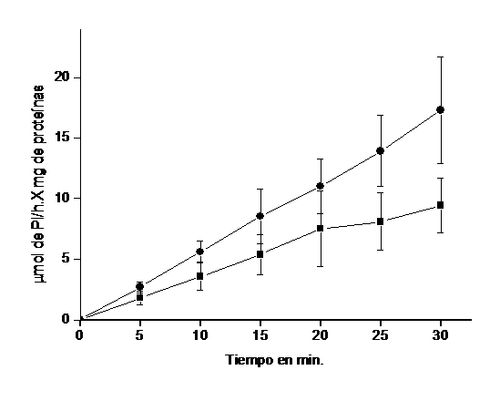
Figura 4. Efectos del
extracto acuoso de las hojas de B.
megalandra en la actividad de la
G-6-Pasa durante el tiempo. La actividad de la G-6-Pasa microsomal hepática
fue medida en la ausencia (■) o en la presencia de 0,28 UA264 nm del
extracto de las hojas de B. megalandra (●)
usando 15 mM
de G-6-P como substrato. Cada punto representa el promedio de 5 experimentos ±
la desviación estándar. Todas las diferencias observadas entre las actividades
de la enzima incubada en la ausencia o presencia del extracto de las hojas
fueron estadísticamente significativas a p< 0,02; con la excepción de la
obtenida a los 20 min. que no fue estadísticamente significativa.
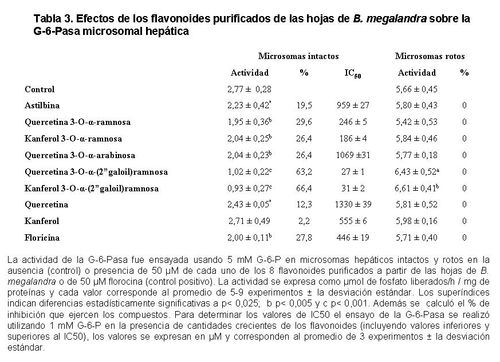
Purificación de flavonoides de B. megalandra y cuantificación de sus
efectos.
A partir del extracto metanólico de las hojas
frescas de B. megalandra logramos
purificar 8 flavonoides (10), la mayoría de ellos como quercetina y
kanferol o sus derivados y se midió el efecto que estos compuestos ejercen
sobre la actividad de la G-6-Pasa.
Las agliconas mostraron la menor actividad inhibitoria, los compuestos
glicosilados con ramnosa presentan una actividad intermedia y cuando la ramnosa
se encuentra esterificada al ácido gálico, la inhibición supera el 60 %. Vale
la pena destacar que el efecto inhibitorio solo se observa en los microsomas
intactos (Tabla 3) lo cual sugiere fuertemente que estos flavonoides afectan
uno de los transportadores, probablemente T1, del sistema de la G-6-Pasa. Hasta donde sabemos, esta es
la primera vez que se describe la presencia de kanferol 3-O-α-(2"galoil)-ramnosa
como producto natural cuya estructura, conjuntamente con la de quercetina
3-O-α-(2"galoil)-ramnosa, se muestra en la Figura 5
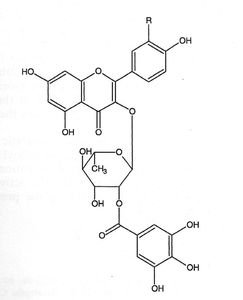
Figura 5. Estructura química de la Quercetina
3-O-α-(2"galoil)ramnosa (R = OH) y del Kanferol 3-O-α-(2"galoil)ramnosa (R = H)
Se encontró una correlación entre el %
de inhibición de la actividad de la
G-6-Pasa de microsomas intactos y el valor del IC50
ejercidos por los compuestos estudiados; las agliconas: kanferol y quercetina,
la quercetina glicosilada con arabinosa (una pentosa) y la astilbina presentan
valores de IC50 elevados y porcentajes de inhibición bajos; la
quercetina y el kanferol glicosilados con ramnosa (una hexosa) poseen valores
intermedios de IC50 y porcentajes de inhibición intermedios y los
flavonoides unidos a ramnosa y ácido gálico exhibieron IC50 del orden
de 30 μM y mostraron inhibición de la actividad de la enzima cercana al 60 %. Se
utilizó como control positivo floricina, un conocido inhibidor de T1 de la
enzima (11), el cual mostró un efecto inhibitorio similar al
ejercido por el kanferol y la quercetina unidos a ramnosa pero un valor de IC50
(466 μM) el cual es cercano al doble del mostrado por los primeros; siendo la
primera vez que se reporta el IC50 de la floricina para la G-6-Pasa de microsomas
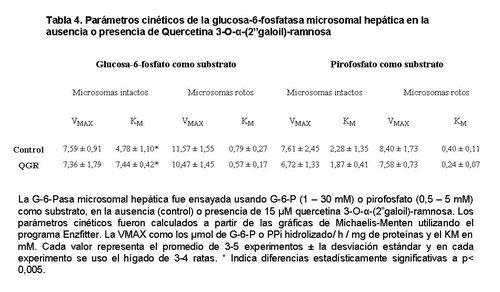
intactos. Como se muestra en la
Tabla 4, quercetina 3-O-α-(2"galoil)-ramnosa (QGR) incrementó
considerablemente el KM para G-6-P sin modificar la VMAX de la G-6-Pasa de microsomas
intactos, tampoco afectó los parámetros cinéticos de la enzima de microsomas
rotos. Cuando se usó PPi como substrato (Tabla 4), los parámetros cinéticos de la G-6-Pasa tanto de microsomas
intactos como rotos no fueron afectados por la presencia de QGR. Estos
resultados sugieren fuertemente que QGR es un inhibidor competitivo del
transportador T1 del sistema de la
G-6-Pasa (12). La
capacidad neoglucogénica de rebanadas de hígado de ratas ayunadas por 48 horas
e incubadas en la ausencia (control) o presencia de 30 μM QGR se muestra en la Fig. 6.
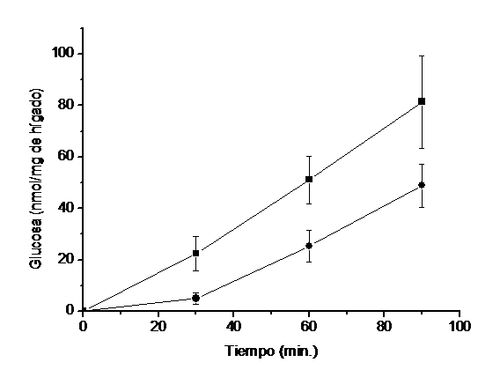
Figura 6. Efectos de la quercetina
3-O-α-(2"galoil)-ramnosa sobre la neoglucogénesis hepática. Rebanadas de hígado de ratas ayunadas por 48 h. fueron incubadas en
amortiguador Krebs-Ringer bicarbonato suplementado con albúmina bovina saturada
con oleato y usando lactato como substrato neoglucogénico en la ausencia (■) o
presencia de 30 μM QGR (●). A los intervalos de tiempos indicados se tomó
muestras del medio de incubación con la finalidad de estimar la glucosa
producida por el método de glucosa oxidasa-peroxidasa (29). Los valores se
expresan como nmol de glucosa producidos por mg de peso seco de hígado y
corresponden al promedio de 6-9 experimentos ± la desviación estándar. Todas
las diferencias entre las rebanadas controles y tratadas con QGR fueron
estadísticamente significativas a p< 0,005.
La producción de
glucosa por las rebanadas controles fue prácticamente lineal y muy similar a lo
reportado antes (9). QGR inhibió drásticamente la capacidad neoglucogénica
de rebanadas de hígado de ratas a todos los tiempos estudiados: a 30 min. la
inhibición fue de aproximadamente 85 %; cercana al 50 % a los 60 min. y de un
41 % a los 90 min. Aun cuando la inhibición de la capacidad neoglucogénica de
las rebanadas de hígado por la presencia del flavonol en el medio de incubación
parece disminuir con el tiempo de incubación, sin embargo una observación
detallada de la Fig.
6 muestra que la pendiente de la línea que representa el efecto del flavonol,
luego de los 20 min. iniciales, es 0.74 lo cual es considerablemente menor que
0.97 de la condición control.