Las enfermedades tropicales desatendidas, THA entre ellas, necesitan
sin duda más atención. Por ello es necesario allanar la distancia entre los
hallazgos del laboratorio y las necesidades de los pacientes; la inequidad en
salud que significa no hacer esto implica que las soluciones al reto, deben
salir de enfoques no convencionales, donde los esfuerzos combinados de la
academia y la industria farmacéutica puedan constituir una esperanza para
disminuir el sufrimiento de las personas afectadas por esta enfermedad, sin
olvidar el concepto moral de equidad de distribución y suministro de servicios
de salud.
Durante los
últimos doce años, en un consorcio de proyectos multicéntricos, liderado por
los Prof. Jörg Hacker, Ulrike Holzgrabe y Gerhard Bringmann, llevados a cabo
principalmente en la Universidad de Würzburg, Alemania y financiados por el
Consejo Alemán de Investigación y Desarrollo (en alemán, DFG), pero con una red
de colaboración extendida a lo largo de muchos países, incluyendo Venezuela,
nos hemos dedicado a la síntesis de compuestos de novo, y semi-síntesis a partir de compuestos naturales activos,
potencialmente útiles, como cabezas de series en el diseño de nuevos
medicamentos en contra de estas tripanosomiasis. El trabajo fue coordinado
entre más de 12 laboratorios universitarios distribuidos en las Facultades de
Química, Medicina, Farmacia y Biología, un laboratorio central de análisis de
los compuestos sintetizados, y más de 100 personas interactuando para diseñar y
probar compuestos en contra de 11 agentes patógenos, entre ellos compuestos
tripanocidas.
Nuestra
orientación ha sido básicamente reconocer que los compuestos que son potentes
en el laboratorio, no necesariamente son los mejores medicamentos en el mercado.
Por ello hemos ahondado esfuerzos con el objetivo de describir herramientas
fundamentales para refinar la selección de candidatos potencialmente aptos para
entrar en estudios preclínicos. Así, inicialmente, se evaluaron miles de
moléculas de diferentes clases estructurales, sintetizadas en el marco de nuestra
plataforma, para determinar sus actividades tripanocidas, su citotoxicidad
contra células de mamíferos y su índice de selectividad. Posteriormente se seleccionaron
185 de ellas y se determinó la correlación entre su eficiencia de ligazón y sus
propiedades químicas estructurales (23). Seguidamente, escogimos 7
compuestos, los más promisorios, y evaluamos, por una parte los cambios
morfológicos producidos por estos compuestos a nivel ultrastructural en el
parásito, así como la correlación de estos cambios con sus propiedades químicas,
a fin de orientar la investigación hacia cuales organelos celulares podrían
constituir los blancos de estos compuestos (23).
El PSA (Polar
Surface Area o área de superficie polar) de una molécula puede ser definido
como la suma de la superficie molecular de los átomos polares, principalmente
oxígeno y nitrógeno, también incluyendo sus hidrógenos unidos (24).
El PSA es una herramienta de uso común en la química medicinal, útil en la
optimización de la capacidad de un fármaco para penetrar las células, y también
en la predicción de las propiedades de Absorción, Distribución, Metabolismo
y Excreción
(ADME) de las moléculas (25, 26, 27, 28). De hecho, está claramente
definido que las moléculas con PSA superior a 140 Å2 tienden a ser poco
transportadas a través de las membranas celulares (28).
En un
esfuerzo por aumentar la validez de nuestro análisis previo (23), y
con el fin de obtener información adicional sobre las características ADME de
los compuestos, determinamos la correlación entre la actividad tripanocida de
los compuestos seleccionados [IC50] (listados en la tabla 2) y su PSA predicho.
Este es un ejemplo de las herramientas
utilizadas para la comprensión de la relación entre la
potencia de un compuesto y sus características químicas en el marco del
proyecto multicéntrico.
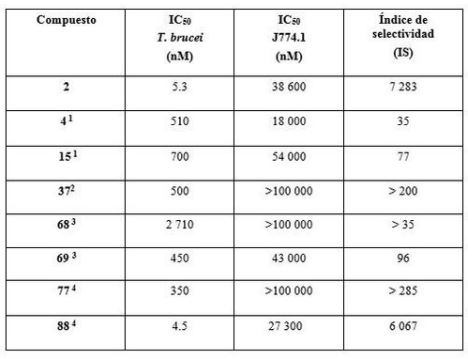
Tabla 2. Actividad tripanocida,
citotoxicidad e IS de compuestos seleccionados.
1Derivados
tipo amino ácido del ácido fumárico y de piperazina.2 Bisnaphthalimidasbisquaternarias. 3 Derivados de piperidine.
4 Sales de N-Arylpyridinium.
Modificado de (23).
La Figura 1 ilustra
la correlación sigmoidal existente. De hecho, puede observarse que los
compuestos con valores de IC50 en el rango nM (bajos) [sales de N-Arylpyridinium,
77 y 88] presentan
valores de PSA muy pequeños, mientras que los compuestos con IC50 en
el rango alto nM y mM [bisnaphthalimidas bisquaternarias
37, y derivados de piperidina,
68 y 69] tienen valores de PSA que son, en algunos casos, incluso superiores a
140 A2. Este dato sugiere su dificultad de atravesar las membranas
celulares.
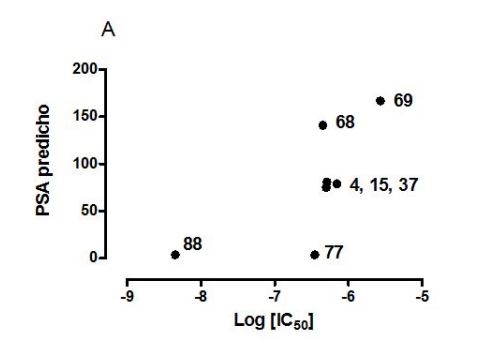
Figura 1.
Correlación entre PSA y log IC50
de los compuestos seleccionados.
Resultados
anteriores obtenidos en el desarrollo de nuestro proyecto indican que [37 y 68]
son promiscuos en el sentido de que tienen afinidad por más de un organelo;
i.e., el retículo endoplasmico y el kinetoplasto (23). El estrés en el
retículo endoplásmico se ha definido como indicativo de toxicidad inducida por
el compuesto utilizado; esto ocurre con más frecuencia en drogas que son
lipofílicas, tienen más de un blanco terapéutico, y presentan una permeabilidad
pasiva significativa (29); este pudiera ser el caso para los
compuestos [37, 68] con PSA en el extremo superior del rango, tal y como ya fue
descrito. Los compuestos [77 y 88],
presentan afinidad por los organelos mencionados y también por el bolsillo
flagelar. Como se definió anteriormente, el estrés sobre el retículo
endoplásmico puede ser un reflejo de toxicidad. Es de hacer notar que [77 y 88]
comparten propiedades fisicoquímicas importantes con el Mitotracker Red®,
compuesto diseñado para marcar fluorescentemente la mitocondria (30).
Sin embargo, su orientación hacia este organelo del parásito pudiera estar
guiada por propiedades como la diferencia de carga, negativa dentro del
kinetoplasto, y su bajo PSA, el cual le otorga propiedades de alta
permeabilidad a través de las membranas (31). Finalmente, las
moléculas con un PSA intermedio [derivados de los amino ácidos del ácido
fumárico y de la piperazina, [4,
15] parecen dirigirse específicamente a espacios ácidos tipo lisosomas(23).
Estos
compuestos, especialmente [15], comparten las propiedades de carga y D de carga con el Lisotracker Red®, un
marcador fluorescente cuyo blanco intracelular son los lisosomas (32).
También el PSA de ambos compuestos se encuentra en el mismo rango del
evidenciado para Lisotracker Red®. Estos datos parecen apoyar la idea de que el
blanco celular de estos compuestos [4 y 15] sean los compartimientos ácidos
tipo lisosoma.
Todo esto
indica que la correlación que existe entre PSA y la actividad de miembros
seleccionados de cada clase de compuesto sobre el parásito T. brucei, forman parte de una prueba de concepto de diseño de
medicamentos y sus características para ser transportados a través de las
diferentes membrana celulares.
Conclusión
La
comprensión de las propiedades ADME de un compuesto, entre ellas las relativas
a la permeabilidad en la membrana, así como las que definen la interacción con
las vías metabólicas u organelos intracelulares influyen en la farmacocinética,
farmacodinamia y mecanismo (s) de acción de los compuestos. Nuestro proceso de
optimización y resultados sugieren que el uso de PSA puede
ser de gran ayuda para comprender la correlación entre la actividad y la
permeabilidad del compuesto. Estos datos son fundamentales para abordar el reto
que significa el incremento del costo del desarrollo de candidatos contra THA.
Agradecimientos
Al Consejo
Alemán de Investigación y Desarrollo (DFG), a la Fundación Alejandro de
Humboldt, Alemania, al Consejo de Desarrollo Científico y Humanístico-UCV y a
la Coordinación de Investigación de la Facultad de Medicina-UCV. A mis
compañeros alemanes por todo su apoyo durante estos doce años de trabajo
conjunto y enriquecedor.