Las nanopartículas son partes de elementos químicos con menos de 100 nm de diámetro, son
destinados a industrias y productos de uso doméstico (oro, plata, cobre,
platino, magnesio, níquel, zinc); se estudian los efectos de ellas en embriones
humanos puesto que atraviesan bien la barrera hematoencefálica fetal y se sabe
de alteraciones que provocan en gran cantidad de procesos metabólicos, a modo
de virus, en el ADN del hospedador, en otras especies.(10, 14-17) De
los fármacos y tóxicos es redundante referirse a ellos como factores que
interfieren el desarrollo normal, al igual que zoonosis parasitarias, virus y
otros patógenos.(18) (Figura 3).
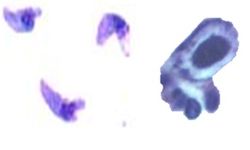
Figura
3. Microfoto. H.E. Izq.: Grupo de taquizoitos de
Toxoplasma gondii, es la forma invasiva y de reproducción asexuada de este
protozoario apicomplexo. Der.: Inclusiones de Citomegalovirus con halo
perinuclear claro típico, en células pulmonares infectadas.
Diferenciación: cuando las
células cambian de forma y de funciones o las adquieren distintas a su
origen-, con memoria que se transmite a las células hijas. Crecimiento es modificación positiva de peso, volumen y/o área; es
mediado por factores de crecimiento (FC): epidérmico, neuronal, de insulina,
fibroblástico, de eritropoyetina, de tejido conectivo, etc. Migración es la cinética resultante de
reubicación celular, ocurre por adherencia o por reconocimiento celulares; para
ello la fibronectina guía el traslado y el colágeno revela el sitio definitivo;
la adhesividad depende de moléculas glicoproteicas de adhesión que desaparecen
al inicio de la migración y se activan al llegar al sitio de destino.(19,
20)
Inducción es cuando las células o estructuras embrionarias influyen
para que otras se diferencien o mueran, por ejemplo, la proteína FRA-2 induce
la diferenciación de queratinocitos a células constituyentes de la epidermis.(21)
Son inductores neurales: el ácido retinoico, el factor de crecimiento
fibroblástico, el factor de crecimiento transformador (TGF) que incluye a las
proteínas BMP o morfogenéticas óseas, el factor Sonic hedgehog que actúa
también en la diferenciación neuronal motriz de astas anteriores medulares, el
TGF-B que hace lo mismo con las neuronas de las posteriores.(22-25)
Los mecanismos de inducción
necesitan de un control o señalización endógena, molecular, la cual es también
controlada genéticamente, sirven para que la señal llegue a su sitio diana y
que lo haga en el tiempo adecuado y con la duración apropiada; se vale para
ello de activación o inhibición según el caso, de receptores, proteincinasas,
tirosincinasas, serina treoninacinasas, presencia de gradientes de difusión,
reconocimiento de la diana específica, mediación de señalizadores como nogina y
cordina, etc.
La apoptosis o muerte programada permite que otro grupo celular
sobreviva, ejemplos: parte de cola embrionaria, las formaciones faríngeas,
parte de notocorda; hay varios inductores de apoptosis conocidos:
mitocondriales (regulados por proteínas proapoptósicas Bcl-2 y otras),
extracelulares (factor de necrosis tumoral, por ejemplo) y factores que la
controlan, como el complejo cisteinil-aspartato, y otras proteasas que activan
a las endonucleasas.(26, 27)
Aunque todas las células
tienen el mismo cariotipo (salvo los gametos), las características propias de
cada espécimen (expresión genética)
permite la diferenciación celular con diversidad citológica y funcional; frecuentemente
se producen cambios heredables que modifican la expresión de los genes sin
alterar la secuencia del ADN, esas innovaciones estudiadas por la Epigenética y que pueden persistir en varias generaciones- pueden deberse a factores ambientales que van
desde la dieta, las adicciones, las enfermedades a las que se exponen,
influencia geográfica o la polución del medio (es decir, causas ambientales),
hasta la edad o el sexo. La expresión genética es un proceso esencial para
mantener la diferenciación de las células, tanto en su estructura como en su
función pues cuando ellas nacen portan el mismo contenido genético, pero al
desarrollarse divergen hasta convertirse en células diferentes debido, en
parte, a los cambios epigenéticos de su ADN.
Los cambios epigenéticos en el
neurodesarrollo temprano ocurren por modulación de la actividad de genes: activación
o inactivación de la transcripción de uno o varios genes o grupos de ellos
silenciados cuando otros están expresándose en
ciertos períodos de tiempo, los más comunes son la metilación -que inhibe- y
acetilación -que dinamiza- de aminoácidos de histonas (proteínas que forman el nucleosoma o eje de
arrollamiento del ADN dentro de cromosomas) y la metilación del ADN.(28,29)
La metilación del ADN es un
proceso reversible mediante el cual la codificación genética puede ser
interpretada de diferente manera según la etapa del desarrollo (30,31);
es regido en buena parte por el gen methyl-CpG binding protein 2 (MECP 2) que
muestra una normal variabilidad según el género, a nivel autosómico.(32,33)
Las uniones entre citosina y guanina (dinucleótidos CpG) son más
abundantes en las áreas de inicio de transcripción génica (islas CpG), si allí la citosina se
metila temporalmente a
5´-metil-citosina, se inactiva el proceso (28,29); esa misma
metilación también influye en cambios trofoblásticos que culminan al lograr
formarse la placenta, por lo que es un factor importante en la implantación del
cigoto en el fondo uterino.(34) Actualmente se usan y siguen
desarrollándose fármacos con principios epigenéticos para modificar
metilaciones y acetilaciones en el transcurso de algunas enfermedades
oncológicas.
Por otra parte, el medio
interno debe mantener normal variabilidad de algunos elementos orgánicos: la
disminución de la concentración de una molécula lipídica esteroidea hidrófoba,
el colesterol neuronal hipocampal, está relacionada con el envejecimiento de
esa estructura, sospechándose ahora que esto juega importante papel en la
apoptosis temprana, así como también en las dificultades de aprendizaje y
memoria de la senectud.(35) (Figura 4).

Figura 4. Molécula de colesterol, con cuatro carbociclos que
forman un complejo ciclopentanoperhidrofenantreno con una cabeza polar (OH, a
la izquierda) y una cola apolar de núcleos condensados, en el otro extremo.
La embriogénesis entonces se
inicia al fusionarse el núcleo del espermatozoide con el del óvulo. Por lo
anteriormente descrito, las células del nuevo ser vivo pasan por etapas de proliferación en número, migración hacia su destino final, diferenciación hacia su aspecto
definitivo, crecimiento en tamaño y maduración hasta lograr plenamente sus
características funcionales.
La diferenciación ocurre
porque hay gradientes de información posicional (concentraciones distintas
moleculares) que son las que gobiernan la formación y evolución de nuestra
simetría bilateral y nuestros ejes ánteroposterior y cráneocaudal; es influida
por el medio interno (fármacos y otras sustancias químicas o biológicas,
hormonas, etc.) y externo (radiaciones) por ser parte de un sistema biológico,
es interdependiente y simultáneo, como lo es también el posterior
neurodesarrollo entendido como el desarrollo psiconeurológico, con la conducta
y cognición siguiendo al desarrollo de la motricidad-.(36,37) Por
diferenciación es que hay diversidad celular y de tejidos. (Figura 5).
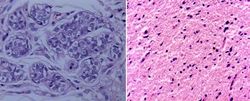
Figura
5. Microfoto. H.E. Tejidos diferenciados: epitelial
glandular (Izq.) y nervioso (Der.).
El desarrollo humano normal tiene tres
períodos: preembrionario, embrionario y fetal; clásicamente, se ha utilizado
los Estadios Carnegie que toman en
cuenta el día del desarrollo, los cambios ocurridos y la longitud en
milímetros, se enumera desde el estadío 1 que es cuando el óvulo es fertilizado
(primer día), la fase de mórula los días 2 y 3 (estadío 2), y así
sucesivamente, hasta el día 57 con cabeza redonda y párpados fusionados,
correspondiente al estadío 23, con 27-31 mm.(38) También se usan para
medir la cronología del desarrollo temprano al número de somitas: a los 20 días
hay entre 1 y 4 somitas, día 21: 4-7, 22: 7-10, 23: 10-13, 24: 13-17, 25:
17-20, 26: 20-23, 27: 23-26, 28: 26-29, 29: 29-34, 30: 34-35 somitas.(5)