Dermatología
Estado actual de terapias CRISPR: nueva esperanza en el armamento dermatológico
Introducción
El manejo de las enfermedades cutáneas incluye el
manejo de los síntomas más que de la causa, siendo estas soluciones a corto
plazo para enfermedades crónicas, con riesgo de desarrollo de efectos adversos,
como infecciones y disrupción de barrera cutánea por lo que surge la necesidad
de desarrollar y aplicar terapias dirigidas a la causa subyacente. Considerando
que la mayoría de las enfermedades cutáneas surgen de mutaciones en el ADN se
plantea la incorporación de terapias CRISPR como una nueva esperanza en el
armamento dermatológico.
El sistema CRISPR, cuyas siglas en inglés se traducen
en Repeticiones palindrómicas cortas agrupadas y regularmente
interespaciadas, se observó por primera vez en genomas de arqueas a finales de
1980. Sin embargo, posteriormente fue detectado en una amplia gama de
microorganismos bacterianos, por lo que son comunes en procariotas. (1)
Característicamente este sistema son secuencias de ADN
cortas (23-45bp de largo); palindrómicas porque los nucleótidos que la conforman se leen igual del extremo 5 a 3 y del
3 al 5; repetidas en una región genómica, agrupadas ordenadamente e
interespaciadas regularmente por secuencias que no son iguales entre ellas
mismas. (1)
Estas secuencias interespaciadoras son iguales a regiones o secuencias
de ADN pertenecientes a bacteriófagos, las cuales fueron adquiridas durante una
infección primaria, e incorporadas al genoma bacteriano por el complejo
Cas1-Cas2. Conociendo este proceso
como adaptación o adquisición. (1)
Las secuencias CRISPR y las secuencias espaciadoras se transcribirán
como un solo ARN, llamado pre-crARN. Posteriormente, se transcribirán los ARN
transactivadores (tracrARN) los cuales acudirán al pre-crARN participando en su
maduración. (1)
Seguidamente una ribonucleasa III separa las secuencias de este crARN,
en secuencias crARN más pequeñas, con secuencias espaciadoras individuales. Siendo este el proceso de expresión.(1)
Finalmente, una proteína o enzima Cas se transcribe y forma un complejo
con la secuencia crARN, formando el complejo de interferencia CRISPR/Cas. (1)
Durante una próxima infección por el mismo fago o
plásmido, el material viral interactuará con el complejo CRISPR/Cas que posee
la secuencia espaciadora de este bacteriófago. La secuencia viral bicatenaria
posee una secuencia PAM (Motivo adyacente de protoespaciador) en el extremo 3.
Estos PAM solo se encuentran en el material genético viral y el sistema CRISPR/Cas
debe reconocerlo para activarse. (1)
Al reconocer estos PAM el complejo comienza a separar
la hebra bicatenaria del material viral y las enzimas Cas utilizan su actividad
de endonucleasa, cortando o degradando el material viral e inactivándolo. (1) (Figura 1)
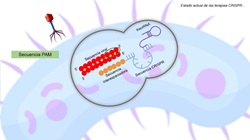 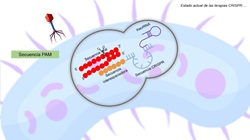 Figura
1. Mecanismo de acción del sistema CRISPR/Cas
De esta manera, se observa que el sistema CRISPR/Cas
le confiere a la célula una forma única y hereditaria de inmunidad adaptativa. (1)
Durante los últimos 15 años se ha avanzado en la
comprensión de las funciones alternativas del sistema CRISPR/Cas. (1)
Dentro de sus funciones, además de la inmunidad
adaptativa, se encuentran la modulación de la fisiología celular, virulencia y
comportamiento bacteriano, incluyendo la formación del biofilm,
regulación de genes y remodelación del genoma. (1)
Dado el creciente potencial del sistema CRISPR/Cas el
campo de aplicación es amplio e incluye inhibición de transferencia horizontal
de genes, tipificación de especies bacterianas, y edición genética. (1)
A través de sistema CRISPR mediado por Cas9 se logran
introducir roturas en el dsDNA de células de mamíferos, utilizando RNA de guía
única (sgRNA), portador de una secuencia complementaria a la secuencia
objetivo, logrando modificar esta secuencia. Esto ha permitido plantear el uso
del sistema CRISPR/Cas para el tratamiento de enfermedades cardiovasculares,
trastornos genéticos, autoinmunes, oncológicos, inflamatorios, bacterianos,
incluso para desarrollar vacunas contra SARS-CoV-2. (1)
Debido a los avances en estudios genéticos y biología
molecular se sabe que las enfermedades cutáneas derivan de cambios en el ADN.
Tal es el caso de las genodermatosis como epidermólisis bullosa e ictiosis
congénita, en donde ocurren mutaciones genéticas monogénicas, por lo que han
sido modelos para la aplicación de terapias de edición génica en modelos
murinos y celulares. (5)
CRISPR y las nucleasas asociadas a CRISPR (Cas)
permiten la edición de objetivos moleculares precisos, secuencias de ARN o ADN,
por lo que este grupo de enfermedades han sido modelo para la aplicación de por
CRISPR/Cas9.(4) (5)
Hasta la fecha los ensayos clínicos de terapia génica
en las genodermatosis se centran en epidermólisis bullosa (epidermólisis
ampollosa de la unión y epidermólisis ampollosa distrófica recesiva o RDEB) y
síndrome de Netherton. (4)
Dada todas las consecuencias derivadas de la edición
génica como mutagénesis insercional, las terapias de edición génica en RDEB
deben ser de alta precisión mediante el empleo de nucleasas como nucleasas
efectoras similares a activadores de transcripción (TALEN) y por supuesto,
CRISPR/Cas. (6)
En un estudio realizado por Bonafont y colaboradores
en el año 2019 se demuestra la eficacia y seguridad de una terapia que emplea
Cas9 guíado por sgARN administrado en forma de ribonucleoproteína por
electroporación para extirpar con precisión el exón 80 del gen COL7A1 que porta
la mutación en la RDEB, incorporando intrones funcionales de donantes. Se
confirmó la restauración adecuada estudiando la transcripción de COL7A1
mediante RT-PCR, demostrando la prevalencia de transcritos que carecen de E80
en células editadas. (6)
Las limitaciones del sistema CRISPR/Cas9 incluyen la
división inespecífica en sitios no deseados (actividad fuera del objetivo) que
sean similares a la secuencia objetivo. Sin embargo, no existen herramientas
para predecir si esto ocurrirá, pudiendo conducir este error a mutaciones o
reordenamientos inesperados que pueden culminar en oncogénesis. (4)
CRISPR/Cas tiene el potencial de revolucionar la
terapia celular y génica para la genodermatosis, siempre que las limitaciones
actuales sean superadas. (4)
Al conocer que las genodermatosis presentan mutaciones
genéticas monogénicas, que son blanco terapéutico en dichas terapias de edición
génica por CRISPR/Cas, surge el interés por conocer en cuáles otras
enfermedades dermatológicas pudieran ser manejadas con edición génica. |