Las úlceras son una discontinuidad de la
barrera epitelial, consiste en una herida convexa de bordes irregulares. Puede
ser superficial afectando la epidermis o profunda dañando tejido nervioso y
muscular, hasta exponer el hueso en el área de la lesión.(7)
Úlceras Vasculares
Heridas causadas por insuficiencias vasculares, donde el flujo sanguíneo
se ve comprometido, concluyendo en isquemia del tejido.
1.- Arteriales
Las
úlceras arteriales también conocidas como úlceras isquémicas, son causadas por
insuficiencias arteriales. Generalmente ocurren en pacientes mayores de 50
años, ocasionalmente son encontradas en pacientes más jóvenes con Diabetes
Mellitus o hiperlipidemias. Son más comunes en hombres, sin embargo, fumar y
algunos factores nutricionales aumentan la incidencia en mujeres.(8)
La
interferencia del flujo sanguíneo puede ser extramural, debido al choque con el
tejido cicatricial (ejemplo: vasculitis o ateroesclerosis), o intramural
(ejemplo: trombosis). El flujo sanguíneo cutáneo se hace inadecuado y no
satisface las demandas metabólicas del tejido local, dañando la piel.
2.- Venosas
En la insuficiencia venosa crónica (IVC), la pared
venosa sufre cambios estructurales y funcionales. El vaso se engrosa y deforma
con aumento en su permeabilidad y pérdida de sus propiedades antitrombóticas.
Como consecuencia de la hipertensión venosa mantenida se altera la microcirculación,
provocando la aparición de lesiones. Además es la causa más frecuente de
úlceras en las piernas, aproximadamente en el 1% de la población.(9)
Los procesos subyacentes a
la IVC, como las zonas cutáneas denominadas dermatosclerosis, culminan en la
degeneración de las células de la piel, del tejido celular subcutáneo e incluso
de la fascia, musculatura, tendones y tejido óseo, y se desarrolla una herida
crónica con escasa tendencia a la curación espontánea.(10)
Las
venas varicosas que aparecen como consecuencia de la insuficiencia del sistema
venoso superficial, presentan cambios estructurales importantes que se asocian
a modificaciones funcionales. En estas modificaciones adaptativas
estructura-función juegan un papel muy importante factores de origen
endotelial, así como interacciones del endotelio con células sanguíneas y con
las células musculares lisas (SMC, del idioma inglés) de la pared del vaso.(9)
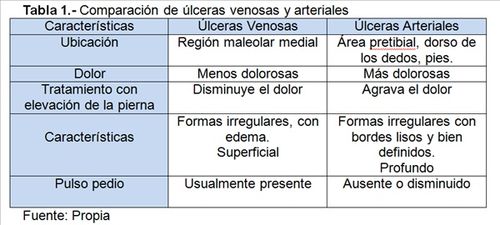
En
la tabla 1 se indican características diferenciales entre úlceras arteriales y
venosas.
En la actualidad se sabe que muchos de los
síndromes asociados a la enfermedad venosa de los miembros inferiores,
trombosis, ulceraciones de origen venoso, entre otros; son en gran medida
responsabilidad de las interacciones entre células sanguíneas y el endotelio
venoso. El estudio ultraestructural de la pared venosa insuficiente muestra
cómo sus células componentes tratan de compensar las necesidades de la pared
ante la hipertensión-hipoxia mantenida.(9)
El endotelio participa en la síntesis de elementos
necesarios para contrarrestar la débil contractilidad del vaso, ayudándolo a
cumplir con el retorno venoso comprometido, sintetizando sustancias tales como
factores vasoactivos, mediadores inflamatorios y componentes del tejido
conectivo.
Desde las primeras etapas de la IVC se producen
cambios funcionales en las células musculares lisas, las cuales proliferan
localmente favoreciendo el engrosamiento de la pared. Estas SMC participan en
la producción de grandes cantidades de tejido conectivo y de enzimas
lisosomales degenerativas.
En
la vena varicosa la regulación del tono venoso dependiente de las SMC está
alterada, pues el desarrollo de tejido conectivo produce grandes separaciones
entre las células rompiendo la distribución armoniosa del influjo nervioso.
Como consecuencia las SMC de la vena insuficiente no pueden producir la debida
contracción de la pared.
Las
células endoteliales gracias a su posición de barrera limítrofe entre la sangre
y el vaso están capacitadas para recibir y responder ante señales de su medio
ambiente que constituyen actividades claves para la vida. Se interconectan con
células de la sangre y el vaso a través de comunicaciones autocrinas y
paracrinas que les permiten controlar el metabolismo de la pared respondiendo
rápidamente a necesidades locales.
Los
leucocitos, especialmente los granulocitos, por ser células altamente reactivas
mantienen intensas interacciones con el endotelio, incluso en condiciones
fisiológicas. La elevada reactividad del leucocito determina su participación
en la fisiopatología de las enfermedades vasculares.(9)
Aproximadamente
la mitad de los granulocitos circulantes en el torrente circulatorio se
encuentra vinculado a la pared de los vasos, principalmente a las venas, las
fuerzas de unión son tan débiles que ruedan siguiendo la dirección del flujo a
lo largo de la pared del vaso. Estas interacciones se realizan mediante
moléculas de adhesión de la familia de las selectinas en los leucocitos y
estructuras de carbohidratos de moléculas de adhesión de la familia de las
mucinas en el endotelio.
Se
ha demostrado que las células endoteliales (CE) activadas por hipoxia
sintetizan y liberan factor activante plaquetario (PAF), un mediador
inflamatorio muy fuerte, cuya acción promueve la adhesión firme del leucocito,
su activación y migración posterior al espacio subendotelial. Las moléculas de
adhesión que intervienen en esta unión firme y en la transmigración del
leucocito son integrinas leucocitarias. En neutrófilos y monocitos esta
interacción está mediada por integrinas de la familia de la B2:
LFA-1; mac-1 y la p150. Adicionalmente en los monocitos también interviene la
integrina VLA-4 de la familia B1 y otras integrinas de la B3. Como
contrarreceptor se encuentran en el endotelio ya activado moléculas de adhesión
de la superfamilia de las inmunoglobulinas tales como ICAM-1 y VCAM-1.(9)
La IVC se caracteriza por variaciones en la
expresión de la integrina CD11b/CD18 (MAC-1) y la L-Selectina. Los niveles de
CD11b disminuyen durante la presencia de la lesión. Los niveles de la
L-Selectina aumentan, indicando la activación de los leucocitos en respuesta a
la hipertensión y su consecuente adhesión al endotelio.(11)
La permeabilidad incrementada de los capilares
dañados promueve la extravasación de proteínas plasmáticas, que sobrepasan la
capacidad reabsortiva de los vasos linfáticos, incrementando el riesgo de
infección. Se producen edemas que limitan la microcirculación de áreas vecinas
por compresión externa de la luz de otros capilares no afectados o por la
acción indirecta de mediadores inflamatorios liberados, disminuyendo el riego
sanguíneo de la zona y así el efecto de barrido de los microorganismos
patógenos que pueden colonizar la lesión característica de la IVC.
Después
de un daño importante en la función capilar en la que interviene tanto el
atrapamiento de leucocitos con la consecuente secreción de productos tóxicos
(citocinas, radicales libres de oxígeno, entre otros.), la formación de fibrina y la formación de
edemas por el incremento en la permeabilidad, se produce isquemia local del
tejido.
Las
alteraciones descritas comprometen tanto a los capilares que deben nutrir al
tejido como a las vénulas poscapilares que deben transportar los productos de
desecho de su metabolismo. Cuando un gran número de vasos capilares está
alterado el defecto nutritivo provoca lesiones tisulares características de la
IVC, la dermolipoesclerosis y la úlcera.(9)
Durante el curso de la enfermedad se
presenta enlentecimiento en la cicatrización de las úlceras, esto se debe
principalmente a la hipertensión venosa, ya que los fibroblastos expuestos al
aumento de la presión venosa presentan una morfología atrófica y la producción
de proteínas específicas que sugieren el envejecimiento prematuro de las
células, además de retraso en su crecimiento y expresión de factores de
senescencia, causando la cronicidad de la lesión y la ausencia de la solución
espontánea de la herida.(12)
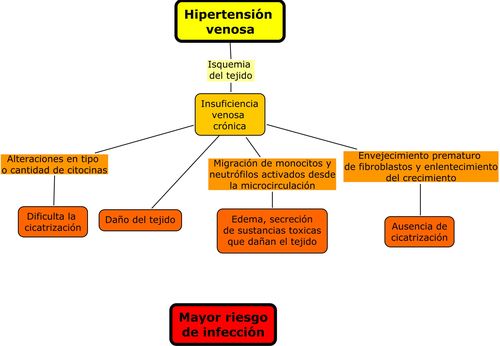
En la figura 1 se esquematiza la
evolución de úlceras vasculares venosas y las relaciones que posibilitan y
favorecen la infección.