Caracterización
morfológica de los quistes
Los aislados A2,
A12, A13, A14, A15, A25, A27, A28, A29,
A30 y A31 fueron incluidos en el grupo II, por presentar quistes con el
ectoquiste plegado. Los aislados A1, A3,
A10, A11, A16, A17, A18, A19, A20, A21 Y A22 se incluyeron dentro del grupo
III, ya que presentaban quistes con el ectoquiste liso. Los quistes de los
aislados A9 y A26 presentaron morfologías compatibles tanto con grupo II y
grupo III, observándose el 60% de los quistes con superficie plegada. El diámetro de los quistes pertenecientes al
grupo II fue en promedio 11,85 µm (Rango: 9,6-14,0 µm), significativamente más
grande (p= 0,035, una cola) que los
del grupo III, los cuales medían en promedio 9,5 µm (Rango: 7,8-10,85 µm).
También se tomó
en cuenta el número de puntas del endoquiste y la cantidad de éstas que hacen
contacto con el ectoquiste. Los aislados del grupo III presentaban muy pocas o
ninguna punta en el endoquiste, por lo tanto no existe contacto con la pared, a
diferencia de los aislados clasificados en el grupo II, en los que se observa
el endoquiste poligonal o estrellado, con 1 a 5 puntas que contactan con el
ectoquiste. La diferencia del valor promedio de las puntas que contactan es
estadísticamente significativo entre ambos grupos (p= 0,005). (Fig.- 1)
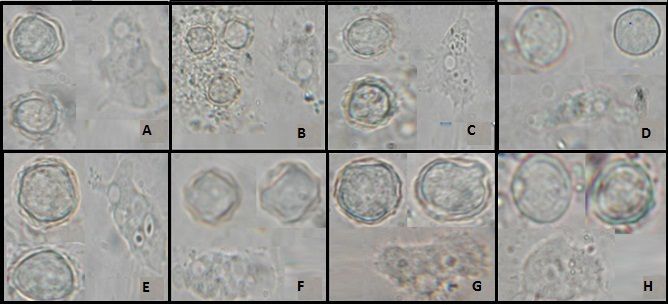
Figura 1.- Trofozoítos y quistes de algunos
aislados de Acanthamoeba spp
pertenecientes al grupo II y III según Pussard y Pons. Examen directo de cultivo en medio
Chinchilla modificado. Objetivo 100x. A: quistes y trofozoítos de A2 B: quistes y trofozoítos de A13 C: quistes y trofozoítos de A14 D: quistes y trofozoítos de A16 E: quistes y trofozoítos de A15 F: quistes y trofozoítos de A29 G: quistes y trofozoítos de A30 H:
quistes y trofozoítos de A21
Caracterización
morfológica de los trofozoítos
Para la
caracterización morfológica de los trofozoítos de Acanthamoeba spp. se
tomó en cuenta el diámetro mayor y menor de los trofozoítos, número de vacuolas
contráctiles, diámetro de las vacuolas contráctiles, pseudópodos emitidos y
número de acantopodios. En términos generales, los trofozoítos clasificados
dentro del grupo II fueron estadísticamente más grandes, tanto en longitud
mayor (LM) (21,7 + 6,3 µm), como en longitud menor (Lm) (11,6 +
3,75 µm) que aquellos que se ubicaron en el grupo III (LM 18,67 + 8,28
µm; Lm 10,28 + 4,27 µm). Se
observó diferencias significativas en el número de pseudópodos emitidos siendo
mayor para los trofozoítos del grupo III (p=0,04). El tiempo de
mantenimiento en el Laboratorio de los aislados del grupo III, fue
significativamente mayor que el de los aislados ubicados en el grupo II (p=
0,020). (Fig.-1)
Clasificación
molecular
Reacción en cadena de la
polimerasa (PCR)
Producto de la amplificación del ADN, se obtienen
fragmentos de 900 pb para los aislados A9, A12, A13, A14, A15, A25, A26, A27, A28, A29, A30 y A31 y de 700 pb para los aislados A1, A3, A10, A11, A16, A17, A18, A19, A20, A21 y A22, lo cual se
corresponde con la existencia de los grupos morfológicos II y III,
respectivamente. Únicamente el aislado A2 clasificado dentro del grupo II
presentó un producto de 700 pb (Fig.- 2)
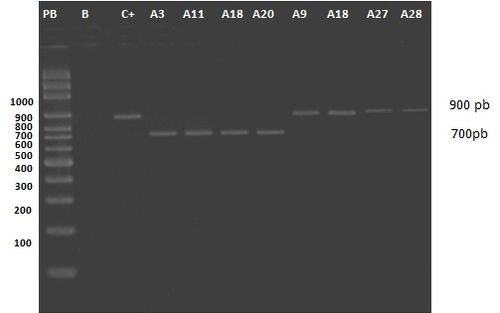
Figura 2.-Productos de PCR de surRNA18 de aislados de Acanthamoeba spp. pertenecientes al
grupo II y grupo III según los criterios morfológicos. PB: Marcador de 100
pares de bases; M: Mezcla; pb: pares de bases producto de RFLP
Al
evaluar la relación entre el tiempo de mantenimiento en cultivo y el tamaño del
producto del PCR obtenido de los aislados de Acanthamoeba spp., se
observó que los aislados con más de 10 años de mantenimiento en cultivo
presentaban productos de 700 pb, mientras que aquellos que tenían un tiempo de
mantenimiento menor a 10 años, presentaban un producto de 900 pb (p=0,007).
RFLP
Una vez
realizada la digestión de los productos de PCR con las enzimas Hinf I, Hha
I y Hae III, solo se pudo identificar el 33% de los aislados estudiados.
Los aislados pertenecientes al grupo III con productos de PCR de 700 pb, no
pudieron ser identificados, por no poder compararse con los patrones de
digestión publicados por Kong y Chung (17).
La caracterización molecular aplicada (PCR-RFLP)
permitió determinar las especies de los aislados A9, A12, A13, A14 como A. polyphaga y la especie de los
aislados A26, A27, A28 y A29 como A.
castellanii. (Fig.- 3)
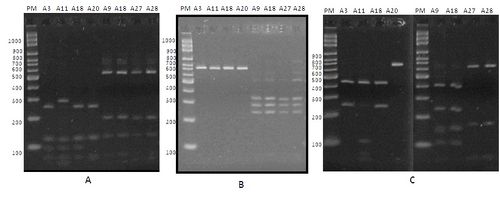
Figura
3. Perfil de digestión del gen de la subunidad ribosomal 18S de los
aislados A3, A11, A18, A20,A9,A18, A27, A28 de Acanthamoeba spp. En el Gel A se observa la digestión realizada
con Hinf I En el Gel B
se observa la digestión realizada con Hha I En el Gel C se observa la digestión realizada
con Hae II Electroforesis en gel de Agarosa al 2,5%, teñido con
SYBER safe (Invitrogen®, USA). PB:
Marcador de 100 pares de bases; M: Mezcla; pb: pares de bases producto del RFLP. C1:control 1- A. castellani
C2: control 2-A polyphaga.
Los aislados
A15, A25 y A30, se identificaron como A. castellanii o A. polyphaga, quedando pendiente su
determinación a través de otras metodologías moleculares.
En lo que respecta a A31, no se obtuvo digestión con
las enzimas seleccionadas, ya que el producto amplificado por PCR no tuvo un
rendimiento adecuado aunque se intentó concentrar el ADN o realizar una
reamplificación de productos anteriores, visualizándose una débil banda de 900 pb
luego de la electroforesis en gel de agarosa al 2,5%.
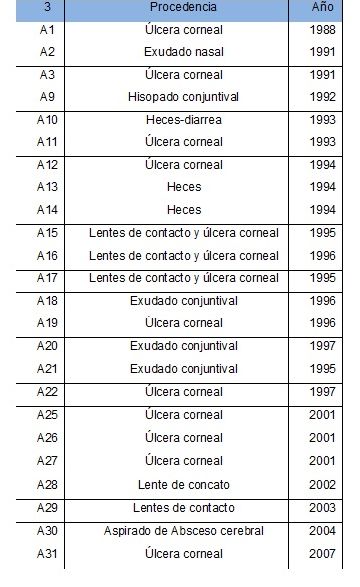
En la Tabla 1 se puede observar los aislados,
producto de PCR e identificación a nivel de especie y relación con el tiempo
que han permanecido en cultivo.
En lo que se
refiere a los resultados de la digestión de los productos de PCR de 700 pb
pertenecientes al grupo III, no se observó correspondencia entre los productos
de digestión con las enzimas Hinf I, Hha I y Hae III y los
patrones publicados por Kong y Chung 1996 (17,18). Sin embargo, se
pudo observar una similitud en los perfiles de digestión obtenidos luego de la
acción de la enzima Hinf I, para los aislados A16, A17 y A10.
Adicionalmente, entre estos últimos y los aislados A19 y A21, hubo una similitud entre 50% y 75%
de los perfiles de digestión.